1.1 スイープテクニック( LSV 、CV、 TAFEL)
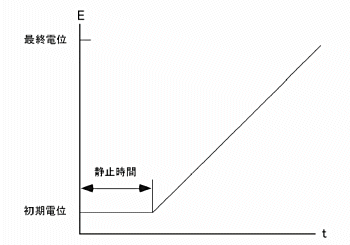
電気化学 測定テクニックの1つ、リニアースイープテクニックでは、電位は一定のスキャン速度で初期電位から最終電位まで直線的に変化させます。電流は印加電位の関数としてモニターされます。簡単なLSV の電位波形を図1に示します。
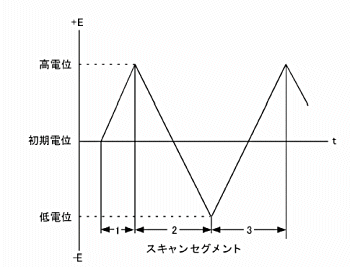
LSV を更に汎用的にしたものがCV です。このテクニックでは、最終電位に達した時、スキャン方向を反転し、同じ電位範囲内で反対の方向に再びスキャンします。フォワードスキャンで生じた電気化学反応の生成物質を逆スキャンで調べることができます。この特徴がCVテクニックが広く使用される主な理由の1つです。CV では、電位は同じ範囲内で何回も繰り返すことができます。初期電位と、スキャンの方向が反転される高電位と低電位の2 つのスイッチングポテンシャル という3つの電位変数の指定が必要です。CV のポテンシャル波形を図.2に示します。
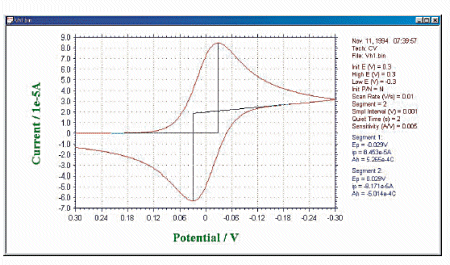
CV の典型的な電流応答曲線(I-E曲線)を図3に示します。 曲線のピークや非対称性は拡散による物質移動により生じます。その他に、曲線の形に影響を及ぼす多数の変数があります。例えば、遅い不均一系の電子移動、酸化或いは還元種の不安定性、吸着などです。不均一系電子移動速度の速い可逆系のCVではピーク電流は下式のRandles-Sevcik 式で表わされます。従って、可逆過程のip は、濃度C とスキャン速度v1/2 に比例します。
ここで ip= ピーク電流(A) 、n=equiv/ モル、A= 電極面積(cm2)
D= 拡散係数(cm2/s)、C= 濃度(mole/cm3) 、v= スキャン速度(V/s)
遅い電子移動速度はピークポテンシャルの分離(対をなす酸化ピーク電位と還元ピーク電位差;Δ Ep)を増加させ、逆に、電子移動の速度定数はスキャン速度によるΔ Ep の変化を調べることにより算出できます。作用電極と参照電極間の未補償溶液抵抗もまた同じくΔ Ep を増加させます。 未補償溶液抵抗の効果はエレクトロニクスによるiR 補償(ポテンショスタットのポジティブフィードバック)により低下させるか、或いは取り除くことができます。
もう1つのCV の用途として電極反応の生成種の反応を研究することがあります。 フォワードスキャンで生じた生成種の反応性は、それ以後に引き続くスキャンにより調べられます。反応速度の定性的評価はスキャン速度を変えて得られます。
CVの持つ簡便性と迅速性という際立った特徴のおかげで、酸化還元系を調べる最初の手段としてしばしば使われ、反応速度とメカニズムの定性的な解析手段として非常に強力なテクニックになりえます。しかし、遅い電子移動効果と化学反応性を切り離すべき方法がないので、CV とLSV は一般に均一系と不均一系の反応速度の定量的な測定には不向きです。 これらの測定には他のテクニック(例えば、クロノクーロメトリー )の方が一般により適しています。とはいえ、他のテクニックが使われる前に、酸化還元電位を知る必要があり、これはCV によって最も便利に調べることができます。
CV とLSV に現われるバックグラウンド(容量性)電流が定量分析手段としての有用性に制限を与えます。一方、 LSV はストリッピングボルタンメトリーによる微量金属の検出に際しては有効な手法になります。酸化種還元種両方が安定(実験のタイムスケール上)であるなら、その時、レドックス過程は電気化学的に可逆的と言れます。そのような系の標準レドックスポテンシャルは2つのピークポテンシャル( Epa と Epc )の平均であり、ピークポテンシャルの差は57/n(mV)です(n は1 モル当たりの移動電子数です)。